Prevela i obradila: Amna Dumpor
Istraživači na Univerzitetu u Helsinkiju otkrili su mehanizam pomoću kojeg se prenose štetni agregati tau proteina između neurona. Pored amiloidnih plakova, tau-agregati u mozgu su značajan faktor u progresiji Alzhajmerove bolesti. Alzhajmerova bolest je povezana sa dvije neuropatologije: amiloidnim plakovima i tau-agregatima, ili tau-proteinom koji se akumulira u neurofibrilarnim snopovima neurona. Amiloidni plakovi mozga su bolje poznata patologija, ali značaj taua u sklopu progresije bolesti je jednako važan.
“Čini se da kod Alzhajmerove bolesti akumulacija amiloida u mozgu počinje prvo, ali simptomi se obično javljaju nakon što amiloidna patologija izazove patologiju taua, pri čemu se izumiranje neuronskih ćelija i gubitak sinapsa počinju ubrzavati”, kaže Henri Huttunen, docent u Centru za neurologiju, Univerziteta u Helsinkiju (HiLIFE jedinica).
“Izgleda da je akumulacija taua stvarno štetan element bolesti.”
Tau se javlja i u zdravim neuronima, ali akumulacija nepravilno preklopljenih, patoloških tau agregata igra ključnu ulogu u Alzhajmerovoj bolesti.
Nova studija otkriva način kako tau agregati prelaze iz ćelije u ćeliju
Ranije se smatralo da tau agregati dobijaju pristup vanćelijskom prostoru samo kada ćelije odumru, ali je u posljednjih nekoliko godina utvrđeno da se taj prelazak patološkog taua ne odvija pomoću molekularnog mehanizma koji pomažu tauu u penetriranju ćelijske membrane.
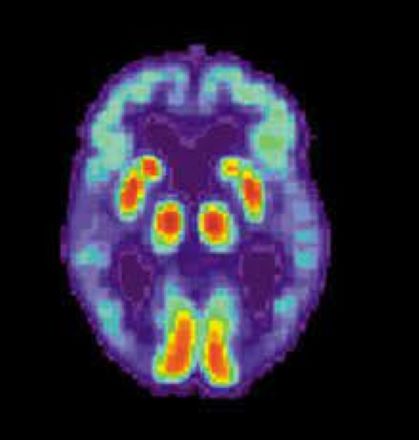
Imidž: Medical Xpress
PET snimak ljudskog mozga zahvaćenim Alzhajmerovom bolešću
Nedavna studija istraživačke grupe Henri Huttunen i Riikka-Liisa Uronena, objavljena u časopisu Cell Reports, ukazuje da akumulacija patološkog taua aktivira sigurnosni ventil u, inače dobro regulisanoj, ćelijskoj membrani. “I kako regulacioni mehanizmi popuštaju, protein tau završava u ćelijskoj membrani. Čini se da lipidni splavovi ćelija obogaćenih holesterolom, igraju centralnu ulogu u ovom mehanizmu tau sekrecije ”, kaže Huttunen.
U istraživanju su korišćeni kultivisani neuroni i prilagođeni proteini da bi se pažljivo posmatrao transfer taua između ćelija.
Uobičajeno, ćelijska membrana čvrsto razdvaja unutrašnje i spoljne dijelove ćelije. Membrana je masna ovojnica, čija je permeabilnost proteina, neurotransmitera i drugih biomolekula pažljivo regulisana.
Najnovija istraživanja daju mogućnost za pronalaženje lijekova za poremećaje memorije
Ovaj pronalazak uvodi novi mehanizam zahvaljujući kojem se farmakološki mogu ciljati određene molekule. Akumulaciju u cerebrospinalnoj tekućini i mozgu se već koristi u dijagnostici bolesti. Molekularni podaci o tome kako tau komunicira sa ćelijskim membranama može se potencijalno koristiti za usporavanje Alzhajmerove bolesti i drugih bolesti koje pripadaju grupi poznate kao tauopatije. Za razliku od amiloidnih plakova, agregati tau proteina se javljaju i kod drugih neurodegenerativnih bolesti, kao što je frontotemporalna demencija.
“Trenutno smo u mogućnosti da liječimo simptome ovih poremećaja, što čini metode liječenja kojim se usporava progresija bolesti važnim ciljem”, objašnjava Huttunen. Neuronske ćelijske membrane sadrže mnogo više omega-3 masnih kiselina od drugih tipova ćelija, a postoje i epidemiološki podaci koji ukazuju na njihov značaj za zdravlje mozga, što se ogleda u trenutnim preporukama o zdravoj ishrani. “Kada se u ćelijske kulture doda omega-3 masne kiseline DHA, tau sekret iz ćelija nestane. Čini se da omega-3 masne kiseline modifikuju mikrostrukturu ćelijske membrane kako bi postale manje propustljive za agregate taua, prikupljajući protein unutar ćelije “, kaže Huttunen.
(Izvor: University of Helsinki, News and Press Releases.)

